Technique de galvanisation à chaud | 2 partie
les reponses a vos questionsUn peu d'histoire
Le terme galvanisation est lié à "l'effet galvanique" et au nom du savant italien Galvani qui a, en particulier, étudié la production d'électricité par le contact de deux métaux de natures différentes. C'est Davy qui lors de l'étude de la pile Zn-Cu de Volta semble avoir proposé pour la première fois l'utilisation du zinc pour "la conservation du fer".
Le procédé de galvanisation à chaud a été inventé par le Français J. Malouin en 1742 puis développé, en France, par Stanislas Sorel, en 1837-42. La première usine a été construite à Solingen, en Allemagne, en 1847.
Actuellement, la galvanisation à chaud est pratiquée selon deux voies :
- - La galvanisation - au trempé - de produits finis.
- - La galvanisation en continu de demi-produits sidérurgiques (tôles, tubes, fils).
Que peut-on galvaniser ?
On peut galvaniser toute pièce en acier susceptible de rouiller : une poutrelle, une cuve, un châssis, un candélabre, un carde -corps…. Pour être galvanisée, la pièce doit cependant répondre aux exigences techniques (cf. conception et normes de galvanisation) et ses dimensions doivent pouvoir entrer dans le bain de zinc . Tous les métaux et alliages hormis l’acier sont exclus . La galvanisation s ’adresse à de plus en plus de corps de métier : charpentiers , constructeurs . Métalliques , pylôniers , chaudronniers, serruriers , agriculteurs, constructeurs automobile…
Pourquoi galvaniser ?
Une duree de vie prolongee
Sans protection, l’acier s’oxyde et entraîne des coûts de maintenance très élevés. La galvanisation à chaud permet de protéger l’acier pour des durées atteignant couramment 25 ans et sans entretien.
Une protection completeLe procédé par immersion dans un bain liquide constitue une garantie totale de protection complète des pièces, même pour les corps creux et tubulaires qui sont protégés à l’intérieur comme à l’extérieur.
Une protection activeLa protection qu’apporte le zinc à l’acier le protége en cas de blessures, rayures ou chocs accidentels ce qui évite toute altération comme les coulures de rouille.
Une resistance aux chocs remarquablesL’alliage fer - zinc formé par la galvanisation est plus dur que l’acier lui même. Il confère au revêtement non seulement une parfaite adhésion, mais aussi une résistance exceptionnelle aux chocs et à l’abrasion.
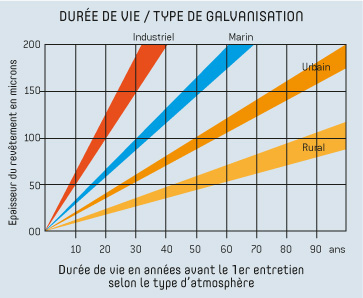 Une excellente tenue a la corrosion atmospherique
Une excellente tenue a la corrosion atmospherique
Le zinc a un comportement très favorable dans l’atmosphère, dans certains types d’eaux, de sols, de produits chimiques et dans le béton. Sa vitesse de corrosion varie selon le type d’atmosphère : milieu marin, urbain, industriel, ou rural.
Un choix economiqueL’acier galvanisé est plus économique que de nombreux systèmes de protection concurrents : Sa longévité supprime les coûts de maintenance.
Un systeme fiableLa galvanisation à chaud est un concept industriel parfaitement maîtrisé qui se réfère à des normes strictes qui garantissent une plus grande fiabilité.
En conclusion
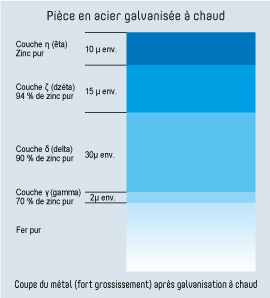 La galvanisation à chaud des pièces manufacturées en alliages ferreux est une opération de revêtement par trempé dans un bain de zinc ou d'alliage de zinc en fusion à une température voisine de 460° C. Le revêtement de zinc couvre les deux faces de l’acier ainsi que l’intérieur et l’extérieur des corps creux. Il forme avec l’acier un alliage résistant et durable qui protège de la corrosion.
La galvanisation à chaud des pièces manufacturées en alliages ferreux est une opération de revêtement par trempé dans un bain de zinc ou d'alliage de zinc en fusion à une température voisine de 460° C. Le revêtement de zinc couvre les deux faces de l’acier ainsi que l’intérieur et l’extérieur des corps creux. Il forme avec l’acier un alliage résistant et durable qui protège de la corrosion.
Pour que la réaction métallurgique entre le Zinc et l’acier se passe dans les conditions optimales, il faut que l’acier soit exempt de salissures telles que la rouille et l’huile. La formation de l’alliage se produit ensuite dans un bain de zinc chauffé à 450°C,Dès que l’acier est à température, la réaction entre le fer et le zinc est immédiate. L’acier est donc trempé successivement dans une solution de dégraissage puis de décapage pour obtenir une surface chimiquement propre. La formation de l’alliage se produit ensuite dans un bain de zinc chauffé à 450°C.Dès que l’acier est à température, la réaction entre le fer et le zinc est immédiate.




